从1964年1月,陆道培院士完成亚洲首例、世界第四例同基因骨髓移植,我国的干细胞临床应用正式破冰,到2025年1月,国家药监局附条件批准中国首款干细胞药物“睿铂生”(艾米迈托赛注射液)上市,我国的干细胞治疗进入产业化阶段,横跨60年的产业之变,让我们看到干细胞产业正全面步入政策合规、技术自主、商业提速的高质量发展新周期。
近日,前瞻产业研究院发布《2025年中国干细胞产业发展白皮书》,从行业发展史及产业链全景、多元化技术路线并行发展与研发转化竞速、产业的竞争格局及未来发展洞察等多维度,深度剖析政策与市场双轮驱动下,干细胞行业规范化深耕、商业化提速的发展现状,全方位洞悉我国干细胞产业的增长新动能与未来新图景。
“一体化”生态格局
迎来新变量
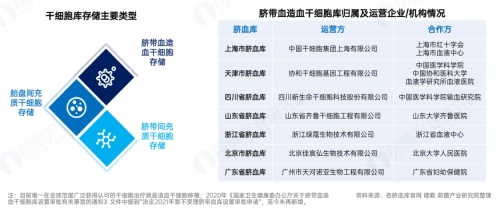
聚焦我国当前的干细胞生态全景,沿全产业链价值逻辑全产业链可分为上、中、下游三大板块:上游立足原材料设备与细胞采集存储,筑牢产业资源底座;中游深耕医疗新技术备案与干细胞药物研发,夯实技术核心竞争力;下游落地临床治疗与健康消费应用,实现产业最终价值交付,全链条协同联动、深度共生。

值得注意的是,在我国干细胞产业链路的布局中,上游产业中的干细胞的采集、制备及储存为我国干细胞最成熟的产业化项目,2025年,该部分的市场规模接近160亿元,占我国干细胞市场总规模的60%。而从这部分的的细分市场来看,脐带血造血干细胞市场受国家严格监管,由拥有牌照的齐鲁干细胞、中源协和等七家“国家队”脐血库运营机构占据;以脐带来源和胎盘来源为主的新生儿间充质干细胞市场也已基本由中源协和、南华生物、四川新生命、博雅干细胞等老牌新生儿储库划分。
中游聚焦医疗新技术备案及干细胞药物研发,当前此环节出现了出现了极具影响力的新变量 —— “818 号令”及“828 号令”,两项新规构建卫健委管技术、药监局管药品双轨监管体系,对干细胞临床研究、技术应用与转化全流程作出刚性规范,同时,完善了干细胞药物研发、注册上市、产业化流通全生命周期管理。中游合规化进程持续提速,将直接赋能下游正规临床治疗与健康消费应用,肃清行业乱象,推动产业全面迈向重研发、重转化、重商业化的高质量转型新阶段。
上中下游的发展是协同共生的,上游储存实力雄厚的头部机构,往往凭借庞大优质的细胞资源储备,在中下游产业布局中占据天然先发优势,形成全链一体化发展势能。如齐鲁干细胞,在以往的行业报告中,我们较少见到它的身影,作为深耕齐鲁的细胞产业,它保持着“山东人”的低调,较少对外发声,但手握国家卫健委、省卫健委认证的“双牌照”,其构建起“1个国家库+5大区域库”的全国性储存网络,坐拥超百万份规模化细胞资源储备,具备强劲底层实力,凭借深厚资源底蕴,近三年加速布局研发与临床转化,无论是在研发管线搭建,还是在临床应用转化落地都快速崛起,行业影响力持续凸显。
“全维度”行业竞争格局
重塑新排位
随着监管体系逐步完善、资本持续涌入、技术不断突破,干细胞行业竞争的核心维度也从资源卡位延向技术、转化、商业化能力的综合比拼,赛道内企业排位正在迎来新一轮洗牌。可以看到当前已逐步形成较为明确的品牌格局,头部企业多为老牌企业,随经验积累建立起较高的行业技术壁垒,例如,中源协和是国内干细胞A股上市领头公司;齐鲁干细胞依托资源库着力打通上中下游产业链;但也不乏快速突围的后起之秀,如源品生物、生创科技、中盛溯源等。

干细胞综合实力TOP10
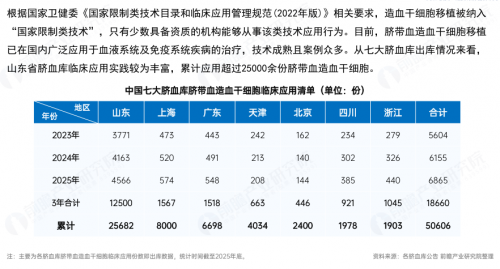
在干细胞市场的细分领域中,造血干细胞是一个特殊板块。依据国家卫生健康委员会《国家限制类技术目录和临床应用管理规范(2022年版)》的相关要求,造血干细胞移植被纳入“国家限制类技术”范畴;而造血干细胞的三大来源分别为骨髓、外周血与脐带血,其中脐带血应由国家批准设立的脐血库提供,这也使得具备合法资质、开展脐带血储存业务的单位形成核心壁垒。从全国七大脐血库的储存及出库情况来看,齐鲁干细胞旗下的山东省脐血库断层式领先,脐带血储存量达93万余份,临床出库量达25000余份(数据统计时间截至2025年底),在强大的资源基础上,质控体系不断升级,成为了我国首个获得国际FACT及中检院双认证的细胞储存机构。
如今正处在干细胞产业的政策关键期,自“818号令”开启政策闸门后,全国范围内干细胞产业竞速态势骤然升温,各地立足自身优势,出台差异化政策、构建特色发展模式,形成多点开花、协同推进的产业格局:山东出台“18条”,从强化创新策源能力、提升临床研究与转化水平、加快产业生态培育、完善创新制度供给四大维度提供全力支持;湖南通过立法推动细胞与基因产业发展;北京构建技术转化、临床加速、产业生态、国际开放、监管创新五重机制;海南博鳌聚焦“先行先试”,以“快”为核心,允许临床项目提前落地;广州主打国际接轨,凭借政策创新吸纳跨国药企布局。

政策向好下,顶层监管框架也更加清晰完善。《生物医学新技术临床研究和临床转化应用管理条例》等多部政策与条例的出台,一方面加速清退不合规中小机构、彻底压缩灰色诊疗空间,推动行业资源持续向头部合规企业集中,行业集中度不断提升;另一方面为长期合规布局的头部机构打通商业化落地通道,此前卡在注册转化环节的研发管线将迎来加速审评上市机遇,整个产业全面迈向重研发、重转化、重商业化的高质量转型新阶段。
干细胞治疗到“ 普惠医疗 ”
到底还有多远?
长期以来,干细胞一直贴着“高端小众”“价格昂贵”“前沿科研”、“离普通家庭遥远”的标签,被视作只有少数人能负担的稀缺医疗技术,难以走进大众生活,而在多部政策与条例的指引下,干细胞正在逐渐迈向“普惠医疗”黄金窗口期。
首先,《生物医学新技术临床研究和临床转化应用管理条例》、《血液系统类医疗服务价格项目立项指南(试行)》等监管政策明确临床研究、技术应用、药品上市全流程刚性规范,让干细胞临床应用有法可依、全程可控、安全可溯,打破大众对行业乱象的顾虑,使其能享受到更安全合规的干细胞服务。
其次,科研管线的推进,让更多疾病得治疗及更多应用场景的实现成为可能。据白皮书统计显示,截至2026年2月底,干细胞医学研究备案项目累计达到185项,重点覆盖神经、心血管、代谢、骨关节及免疫疾病等领域。而干 细 胞 药 物IN D受理仅2025年受理量就达68款,同比倍增,适应症矩阵拓展至逾百种。
最后,就是大众普遍关注的治疗费用与可及性问题,也正随着行业规范化、规模化发展持续改善。2025 年 1 月我国首款自主研发干细胞药物艾米迈托赛注射液(睿铂生)正式获批上市,并于同年 6 月开出首张处方完成首针注射,该药物国内定价约1.98 万元 / 袋,对比美国同类产品近 19 万美元 / 袋的天价,价格降幅超90%。2025年11月、12月,该药相继纳入北京、荆州等地惠民保,最高赔付在60%-70%。同期,5款百万级一针的CAR-T细胞疗法产品首次被纳入国内商保目录。在北海市公布的2026年惠民保保障内容中,就有4款产品赫然在列。
干细胞产业的发展拐点已至,竞速成长正当其时,头部企业引领技术突破,地方布局多点开花,产业发展正加速实现从资源储备向价值落地的跨越,细胞治疗的“昂贵”标签也终将被改写。未来,相信随着技术转化提速、成本优化,细胞治疗将更具可及性,普通大众将能更便捷地享受到安全、高效、可负担的细胞医疗服务,让曾经 “高价” 的生命保障,逐渐走进寻常家庭,成为守护每一位普通人健康的坚实后盾,实现产业初心。
免责声明:此文内容为本网站转载企业宣传资讯,仅代表作者个人观点,与本网无关。文中内容仅供读者参考,并请自行核实相关内容。如用户将之作为消费行为参考,本网敬告用户需审慎决定。本网不承担任何经济和法律责任。
- 热点关注 Hotattention



